
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
Решение. При переходе из начального в конечное состояние объем газа увеличился, газ совершил работу А. Выполняется первый закон термодинамики: переданное газу количество теплоты Q равно сумме изменения внутренней энергии газа ![]() и работы А, совершенной газом.
и работы А, совершенной газом.


Внутренняя энергия идеального газа в

Работа А при переходе газа из состояния 1 в состояние 3 равна площади фигуры под графиком диаграммы в координатах

В результате получаем количество теплоты:

![]()


Положительное значение величины Q означает, что газ получил количество теплоты.
Ответ: 700 Дж.
| Критерии оценивания выполнения задания | Баллы |
|---|---|
| Приведено полное решение, включающее следующие элементы: I) записаны положения теории и физические законы, закономерности, применение которых необходимо для решения задачи выбранным способом; II) описаны все вновь вводимые в решении буквенные обозначения физических величин (за исключением обозначений констант, указанных в варианте КИМ, обозначений, используемых в условии задачи, и стандартных обозначений величин, используемых при написании физических законов); III) представлены необходимые математические преобразования и расчеты (подстановка числовых данных в конечную формулу), приводящие к правильному числовому ответу (допускается решение «по частям» с промежуточными вычислениями); IV) представлен правильный ответ. | 3 |
| Правильно записаны все необходимые положения теории, физические законы, закономерности, и проведены необходимые преобразования, но имеется один или несколько из следующих недостатков. Записи, соответствующие пункту II, представлены не в полном объеме или отсутствуют. И (ИЛИ) В решении имеются лишние записи, не входящие в решение (возможно, неверные), которые не отделены от решения и не зачеркнуты. И (ИЛИ) В необходимых математических преобразованиях или вычислениях допущены ошибки, и (или) в математических преобразованиях/вычислениях пропущены логически важные шаги. И (ИЛИ) Отсутствует пункт IV, или в нем допущена ошибка. | 2 |
| Представлены записи, соответствующие одному из следующих случаев. Представлены только положения и формулы, выражающие физические законы, применение которых необходимо и достаточно для решения данной задачи, без каких-либо преобразований с их использованием, направленных на решение задачи. ИЛИ В решении отсутствует ОДНА из исходных формул, необходимая для решения данной задачи (или утверждение, лежащее в основе решения), но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи. ИЛИ В ОДНОЙ из исходных формул, необходимых для решения данной задачи (или в утверждении, лежащем в основе решения), допущена ошибка, но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи. | 1 |
| Все случаи решения, которые не соответствуют вышеуказанным критериям выставления оценок | 0 |
| Максимальный балл | 3 |








 Дж.
Дж. в результате чего его температура изменилась на некоторую величину
в результате чего его температура изменилась на некоторую величину  в результате чего его температура изменилась также на
в результате чего его температура изменилась также на 








 В этой формуле стоит 5/2 вместо привычных 3/2, это отражает тот факт, что у двухатомных молекул 5 степеней свободы (два вращения + три поступательных движения) в отличие от одноатомных молекул, у которых есть только три поступательных движения. (Замечание: для многоатомных молекул (состоящих из трех и более атомов) справедлива формула
В этой формуле стоит 5/2 вместо привычных 3/2, это отражает тот факт, что у двухатомных молекул 5 степеней свободы (два вращения + три поступательных движения) в отличие от одноатомных молекул, у которых есть только три поступательных движения. (Замечание: для многоатомных молекул (состоящих из трех и более атомов) справедлива формула  так как для них есть шесть степеней свободы: три вращения + три поступательных движения.)
так как для них есть шесть степеней свободы: три вращения + три поступательных движения.)

 и
и  Па — объем и давление газа в состоянии 1. Найдите количество теплоты, сообщенное газу в данном процессе 1–2–3.
Па — объем и давление газа в состоянии 1. Найдите количество теплоты, сообщенное газу в данном процессе 1–2–3.
 а на изохорическом участке 2–3 она равна нулю:
а на изохорическом участке 2–3 она равна нулю:  Как видно из рисунка,
Как видно из рисунка,  и суммарная работа в процессе 1–2–3 равна
и суммарная работа в процессе 1–2–3 равна 
 Согласно уравнению Клапейрона — Менделеева для одного моля идеального газа имеем
Согласно уравнению Клапейрона — Менделеева для одного моля идеального газа имеем  так что
так что  Изменение внутренней энергии газа в процессе 1–2–3 равно, таким образом,
Изменение внутренней энергии газа в процессе 1–2–3 равно, таким образом, 

 и
и 



 Количество теплоты, которое при этом отдается холодильнику, равно
Количество теплоты, которое при этом отдается холодильнику, равно 
 причем все соотношения количеств теплоты, работы и температур остаются такими же, как при работе идеальной тепловой машины в прямом направлении.
причем все соотношения количеств теплоты, работы и температур остаются такими же, как при работе идеальной тепловой машины в прямом направлении.


 где
где 
 Согласно уравнению Клапейрона-Менделеева
Согласно уравнению Клапейрона-Менделеева  откуда
откуда 







 Напишем уравнение Менделеева — Клапейрона для второго и третьего состояний газа:
Напишем уравнение Менделеева — Клапейрона для второго и третьего состояний газа:
 получаем
получаем  Тогда:
Тогда:




 Дж. Участок 3–1 — адиабата. Количество теплоты, отданное газом за цикл холодильнику, равно
Дж. Участок 3–1 — адиабата. Количество теплоты, отданное газом за цикл холодильнику, равно  Дж. Количество вещества газа в ходе процесса не меняется. Найдите работу
Дж. Количество вещества газа в ходе процесса не меняется. Найдите работу 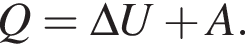
 кроме того его температура растет, а значит,
кроме того его температура растет, а значит,  и
и  следовательно, газ получает тепло.
следовательно, газ получает тепло. 

 Следовательно, газ отдает тепло холодильнику.
Следовательно, газ отдает тепло холодильнику.  Работе газа на диаграмме
Работе газа на диаграмме  Используя уравнение Клаперойна — Менделеева
Используя уравнение Клаперойна — Менделеева  для изменения внутренней энергии на участке 1–2 имеем:
для изменения внутренней энергии на участке 1–2 имеем: 









 Работа газа в данном процессе равна площади трапеции:
Работа газа в данном процессе равна площади трапеции:  Согласно уравнению состояния идеального газа, то есть уравнению Клапейрона — Менделеева, неизвестное давление
Согласно уравнению состояния идеального газа, то есть уравнению Клапейрона — Менделеева, неизвестное давление 









 где
где  отрицательна, поэтому
отрицательна, поэтому 
 Тогда:
Тогда:




 Тогда
Тогда 


 Тогда
Тогда  откуда:
откуда:



 Количество теплоты, переданное тепловой машине в цикле, равно сумме всех положительных теплот:
Количество теплоты, переданное тепловой машине в цикле, равно сумме всех положительных теплот:  Поэтому КПД тепловой машины будет:
Поэтому КПД тепловой машины будет:

 откуда
откуда 
 По первому закону термодинамики теплота, полученная газом, вычисляется по формуле:
По первому закону термодинамики теплота, полученная газом, вычисляется по формуле:

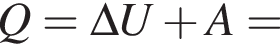










 а ее изменение:
а ее изменение:

 Количество теплоты Q34, отданное при изохорном охлаждении на участке 3–4, равно уменьшению внутренней энергии газа этом участке:
Количество теплоты Q34, отданное при изохорном охлаждении на участке 3–4, равно уменьшению внутренней энергии газа этом участке:
 Отсюда находим:
Отсюда находим: 

 откуда
откуда  Следовательно:
Следовательно:

 где
где  — изменение внутренней энергии газа,
— изменение внутренней энергии газа,  — совершенная газом работа. Из уравнения Клапейрона — Менделеева
— совершенная газом работа. Из уравнения Клапейрона — Менделеева  следует, что:
следует, что:








 и пропорциональна температуре, то в процессе 1–2–3 с одинаковой начальной и конечной температурой ее суммарное изменение ΔU123 = 0.
и пропорциональна температуре, то в процессе 1–2–3 с одинаковой начальной и конечной температурой ее суммарное изменение ΔU123 = 0.






 Согласно первому началу термодинамики
Согласно первому началу термодинамики  где
где  (одноатомный газ).
(одноатомный газ). поэтому:
поэтому:

 получаем:
получаем:
 причем, в замкнутом цикле начальная и конечная температуры совпадают, поэтому за цикл
причем, в замкнутом цикле начальная и конечная температуры совпадают, поэтому за цикл 
























 Работа газа при изобарном процессе
Работа газа при изобарном процессе  изменение внутренней энергии
изменение внутренней энергии  Тогда с учетом уравнения Клапейрона — Менделеева
Тогда с учетом уравнения Клапейрона — Менделеева 



















 Здесь мы считаем все величины положительными, а знаки разных вкладов учитываем при написании уравнений.
Здесь мы считаем все величины положительными, а знаки разных вкладов учитываем при написании уравнений. откуда
откуда  где
где 

 Это очень выгодно по сравнению с простыми электрообогревателями, КПД которых равен единице!
Это очень выгодно по сравнению с простыми электрообогревателями, КПД которых равен единице!
 Затем этот же газ адиабатически расширяется так, что
Затем этот же газ адиабатически расширяется так, что  Отношение модулей работ в изобарном и адиабатическом процессах
Отношение модулей работ в изобарном и адиабатическом процессах  Из уравнения Менделеева — Клапейрона для первого и второго состояния газа
Из уравнения Менделеева — Клапейрона для первого и второго состояния газа  и
и  получаем:
получаем:



 откуда:
откуда:



 откуда
откуда  следовательно, k = 4.
следовательно, k = 4. Затем газ адиабатически расширяется, при этом его температура изменяется до значения
Затем газ адиабатически расширяется, при этом его температура изменяется до значения  Найдите работу газа А2 при адиабатном расширении. Количество вещества в процессах остается неизменным.
Найдите работу газа А2 при адиабатном расширении. Количество вещества в процессах остается неизменным. где р — давление гелия в этом процессе, ΔV — изменение его объема.
где р — давление гелия в этом процессе, ΔV — изменение его объема.
 и его работы
и его работы  Откуда получаем:
Откуда получаем:



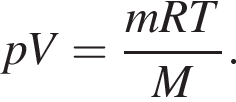 При кипении масса пара увеличивается, температура пара равна температуре кипения и остается постоянной пока весь бензол не выкипит, давление по условию также постоянно. Значит, выполняется соотношение
При кипении масса пара увеличивается, температура пара равна температуре кипения и остается постоянной пока весь бензол не выкипит, давление по условию также постоянно. Значит, выполняется соотношение 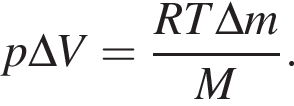
 бензола. Найдем работу, которую совершает пар:
бензола. Найдем работу, которую совершает пар:



 откуда
откуда 
 откуда
откуда 


 откуда:
откуда:



 где
где  Таким образом, как следует из диаграммы процесса:
Таким образом, как следует из диаграммы процесса:







 гелия при температуре t = 17 °C. Если сообщить гелию количество теплоты Q = 3 кДж, то сосуд лопнет. Какую максимальную разность давлений внутри сосуда и снаружи него он выдерживает? Атмосферное давление p0 = 105 Па.
гелия при температуре t = 17 °C. Если сообщить гелию количество теплоты Q = 3 кДж, то сосуд лопнет. Какую максимальную разность давлений внутри сосуда и снаружи него он выдерживает? Атмосферное давление p0 = 105 Па.
 Значит, гелий нагреется до температуры
Значит, гелий нагреется до температуры 
 давление во втором состоянии будет равно
давление во втором состоянии будет равно  Разность давлений снаружи и изнутри равна
Разность давлений снаружи и изнутри равна 


 при температуре кипения t = 80 °C. При сообщении бензолу количества теплоты Q часть его превращается в пар, который при изобарном расширении совершает работу А. Удельная теплота парообразования бензола L = 396 · 103 Дж/кг, его молярная масса M = 78 · 10−3 кг/моль. Какая часть подведенного к бензолу количества теплоты переходит в работу? Объемом жидкого бензола пренебречь.
при температуре кипения t = 80 °C. При сообщении бензолу количества теплоты Q часть его превращается в пар, который при изобарном расширении совершает работу А. Удельная теплота парообразования бензола L = 396 · 103 Дж/кг, его молярная масса M = 78 · 10−3 кг/моль. Какая часть подведенного к бензолу количества теплоты переходит в работу? Объемом жидкого бензола пренебречь. где p — атмосферное давление,
где p — атмосферное давление,  где M = 78 · 10−3 кг/моль — молярная масса бензола, T = 80 + 273 = 353 K — температура кипения бензола. Отсюда
где M = 78 · 10−3 кг/моль — молярная масса бензола, T = 80 + 273 = 353 K — температура кипения бензола. Отсюда 





 давление увеличивается в 2 раза.
давление увеличивается в 2 раза.  или
или 
 или
или 
 откуда T3 = 4T1.
откуда T3 = 4T1.


























 и
и 
 Найдем работу за цикл
Найдем работу за цикл  Для изохорного процесса
Для изохорного процесса  При адиабатном процессе из первого закона термодинамики
При адиабатном процессе из первого закона термодинамики  следует, что
следует, что 
 а изменение внутренней энергии
а изменение внутренней энергии  Для изобарного процесса
Для изобарного процесса  Учитывая, что из уравнения Клапейрона — Менделеева
Учитывая, что из уравнения Клапейрона — Менделеева  Таким образом, работа газа за цикл:
Таким образом, работа газа за цикл:
 но при этом
но при этом  а
а  то от нагревателя получена теплота
то от нагревателя получена теплота 





 то с учетом уравнения Менделеева — Клапейрона
то с учетом уравнения Менделеева — Клапейрона 

 откуда:
откуда:








 и
и  где p0 и V0 — некоторые постоянные величины давления и объема. Какую работу А1234 совершил газ в этом процессе при переходе из состояния 1 в состояние 4, в котором температура газа приняла максимальное значение? Известно, что температура газа в состоянии 2 была равна T2 = 150 К.
где p0 и V0 — некоторые постоянные величины давления и объема. Какую работу А1234 совершил газ в этом процессе при переходе из состояния 1 в состояние 4, в котором температура газа приняла максимальное значение? Известно, что температура газа в состоянии 2 была равна T2 = 150 К.



 и
и 
 работа не совершается: А23 = 0.
работа не совершается: А23 = 0.
 ) на диаграмме равна работе газа, выраженной в единицах
) на диаграмме равна работе газа, выраженной в единицах  поскольку в точке 2 как раз x = 1, V = V0, и y = 1, p = p0, а T = T2.
поскольку в точке 2 как раз x = 1, V = V0, и y = 1, p = p0, а T = T2.

 и
и 
 при xm = 3.
при xm = 3. и (для ν = 1 моль)
и (для ν = 1 моль) 





















 пулеметных лент.
пулеметных лент. а теплота
а теплота  где в силу условия равенства единице числа молей газа величина Ci — это молярная теплоемкость идеального одноатомного газа на данном участке цикла.
где в силу условия равенства единице числа молей газа величина Ci — это молярная теплоемкость идеального одноатомного газа на данном участке цикла. и
и  так что:
так что:


 и на изобарном участке 2–3, где:
и на изобарном участке 2–3, где:
















 Найдите давление газа
Найдите давление газа 


 где
где  так что
так что 









 В эти пары внутрь цилиндра внесли тонкостенный медный стакан массой
В эти пары внутрь цилиндра внесли тонкостенный медный стакан массой  и объемом
и объемом  давно заполненный льдом с температурой
давно заполненный льдом с температурой  Плотность льда равна
Плотность льда равна  Какая масса m паров воды сконденсируется при установлении теплового равновесия в системе?
Какая масса m паров воды сконденсируется при установлении теплового равновесия в системе? и расходуемая на нагревание медного стакана и плавление льда в нем (здесь L — удельная теплота парообразования воды, равная 2,3 · 106 Дж/кг).
и расходуемая на нагревание медного стакана и плавление льда в нем (здесь L — удельная теплота парообразования воды, равная 2,3 · 106 Дж/кг). пары воды в нем все время остаются насыщенными, то процесс нагревания стакана со льдом будет происходить до тех пор, пока сам стакан и вода в нем, получившаяся при плавлении льда, не нагреются до 100 °C. После этого вода в стакане будет находиться в равновесии с насыщенным паром, и процесс его конденсации на стакане закончится.
пары воды в нем все время остаются насыщенными, то процесс нагревания стакана со льдом будет происходить до тех пор, пока сам стакан и вода в нем, получившаяся при плавлении льда, не нагреются до 100 °C. После этого вода в стакане будет находиться в равновесии с насыщенным паром, и процесс его конденсации на стакане закончится.
 в стакане, равно
в стакане, равно  где
где  — удельная теплота плавления льда.
— удельная теплота плавления льда.
 Используя найденные выражения для всех количеств теплоты, окончательно получаем искомую массу сконденсировавшегося пара:
Используя найденные выражения для всех количеств теплоты, окончательно получаем искомую массу сконденсировавшегося пара: 




 одноатомного идеального газа (p и V — давление и объем газа,
одноатомного идеального газа (p и V — давление и объем газа, 


 В соответствии с первым законом термодинамики
В соответствии с первым законом термодинамики  Для изохорного процесса
Для изохорного процесса  для изобарного
для изобарного  Изменение внутренней энергии
Изменение внутренней энергии 

 преобразуем последнее выражение:
преобразуем последнее выражение:







 довели до температуры кипения. Затем начался процесс кипения, и вся эта вода испарилась. На какую величину
довели до температуры кипения. Затем начался процесс кипения, и вся эта вода испарилась. На какую величину 

 воды и табличной удельной теплоты её парообразования
воды и табличной удельной теплоты её парообразования  при нормальном атмосферном давлении
при нормальном атмосферном давлении  и температуре кипения
и температуре кипения  Получаем:
Получаем: 




 подчиняющимся уравнению Менделеева — Клапейрона.
подчиняющимся уравнению Менделеева — Клапейрона. 




 При расширении газ совершает положительную работу, при нагревании внутренняя энергия газа увеличивается, следовательно, газ получает положительное количество теплоты от нагревателя.
При расширении газ совершает положительную работу, при нагревании внутренняя энергия газа увеличивается, следовательно, газ получает положительное количество теплоты от нагревателя. При изобарном процессе работа газа равна
При изобарном процессе работа газа равна  а изменение внутренней энергии одноатомного идеального газа
а изменение внутренней энергии одноатомного идеального газа  где
где  а полученная теплота
а полученная теплота 
 поскольку на участке 2–3 работа не совершается. При адиабатном сжатии по условию
поскольку на участке 2–3 работа не совершается. При адиабатном сжатии по условию  при этом работа газа отрицательна, потому что объем газа уменьшается. Тогда получаем, что работа газа за цикл равна
при этом работа газа отрицательна, потому что объем газа уменьшается. Тогда получаем, что работа газа за цикл равна 

 и
и  Тогда газ совершает положительную работу
Тогда газ совершает положительную работу  Изменение внутренней энергии одноатомного идеального газа в этом процессе
Изменение внутренней энергии одноатомного идеального газа в этом процессе 
 откуда
откуда 
 следовательно, температура газа уменьшается. При изохорном процессе работа газа равна нулю, при уменьшении температуры изменение внутренней энергии идеального газа
следовательно, температура газа уменьшается. При изохорном процессе работа газа равна нулю, при уменьшении температуры изменение внутренней энергии идеального газа  отрицательное. По первому закону термодинамики
отрицательное. По первому закону термодинамики  отрицательно, то есть в этом процессе газ теплоту отдает холодильнику
отрицательно, то есть в этом процессе газ теплоту отдает холодильнику 
 найдем количество теплоты, отданное холодильнику:
найдем количество теплоты, отданное холодильнику:





 и температурой
и температурой 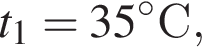 а затем второй вдул туда же объём V2 = 2 л воздуха с относительной влажностью
а затем второй вдул туда же объём V2 = 2 л воздуха с относительной влажностью  и с той же температурой. Какова будет относительная влажность воздуха
и с той же температурой. Какова будет относительная влажность воздуха  Давления насыщенных паров воды при температурах t1 и t2 равны, соответственно,
Давления насыщенных паров воды при температурах t1 и t2 равны, соответственно,  и
и  Изменением объёма пакета при остывании воздуха пренебречь.
Изменением объёма пакета при остывании воздуха пренебречь. откуда
откуда 
 так что вначале надо определить полную массу m воды в пакете после смешивания двух порций влажного воздуха:
так что вначале надо определить полную массу m воды в пакете после смешивания двух порций влажного воздуха: 
 найдём массу насыщенных паров воды в нём при температуре T2, учитывая сложение давлений паров по закону Дальтона:
найдём массу насыщенных паров воды в нём при температуре T2, учитывая сложение давлений паров по закону Дальтона: 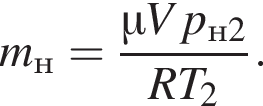






 и
и 











 В состоянии 1 газ находится при нормальных условиях (давление
В состоянии 1 газ находится при нормальных условиях (давление  температура
температура  В состоянии 3 давление
В состоянии 3 давление  а объём
а объём  Найдите, какое количество теплоты
Найдите, какое количество теплоты  к количеству теплоты
к количеству теплоты 






 получаем, что
получаем, что 




 его температура также уменьшается. Тогда газ совершает отрицательную работу, его внутренняя энергия уменьшается. По первому закону термодинамики
его температура также уменьшается. Тогда газ совершает отрицательную работу, его внутренняя энергия уменьшается. По первому закону термодинамики  то есть газ теплоту отдает.
то есть газ теплоту отдает.







 его температура также увеличивается. Тогда газ не совершает работу, его внутренняя энергия увеличивается. По первому закону термодинамики
его температура также увеличивается. Тогда газ не совершает работу, его внутренняя энергия увеличивается. По первому закону термодинамики  то есть газ теплоту получает.
то есть газ теплоту получает.










 При этом газ совершает положительную работу
При этом газ совершает положительную работу  его внутренняя энергия увеличивается
его внутренняя энергия увеличивается  Согласно первому закону термодинамики газ получает от нагревателя количество теплоты
Согласно первому закону термодинамики газ получает от нагревателя количество теплоты
 температура газа уменьшается. Тогда газ работу не совершает, а его внутренняя энергия уменьшается
температура газа уменьшается. Тогда газ работу не совершает, а его внутренняя энергия уменьшается  По первому закону термодинамики газ отдает холодильнику количество теплоты
По первому закону термодинамики газ отдает холодильнику количество теплоты



 Газ теплоту отдает холодильнику.
Газ теплоту отдает холодильнику.

 Газ теплоту получает от нагревателя.
Газ теплоту получает от нагревателя. и
и 
 количество теплоты, отданное холодильнику, равно
количество теплоты, отданное холодильнику, равно 


 и тем фактом, что работа газа в некотором процессе численно равна площади под участком графика, изображающего данный процесс на pV-диаграмме.
и тем фактом, что работа газа в некотором процессе численно равна площади под участком графика, изображающего данный процесс на pV-диаграмме.




 где m — масса угля, сгорающего за один цикл работы двигателя.
где m — масса угля, сгорающего за один цикл работы двигателя.
 Отсюда масса M угля, сгорающего за N циклов работы двигателя, равна
Отсюда масса M угля, сгорающего за N циклов работы двигателя, равна 
